Wasserstoffbrücken
Wasserstoffbrücken sind spezielle intermolekulare Wechselwirkungen zwischen einem Wasserstoffatom und einem stark elektronegativen Atom, beispielsweise Sauerstoff, Stickstoff oder Fluor. Dabei ist das Wasserstoffatom kovalent an ein elektronegatives Atom gebunden und wechselwirkt zusätzlich mit einem freien Elektronenpaar eines benachbarten Moleküls.
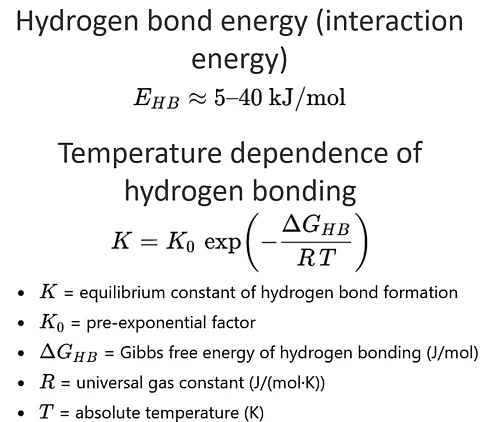
Wasserstoffbrückenenergie (typischer Bereich)
E_HB ≈ 5 – 40 kJ/mol
- E_HB ist die Wasserstoffbrückenenergie
- typische Werte hängen vom Donor-Akzeptor-Paar ab
Temperaturabhängigkeit der Wasserstoffbrückenbindung (Arrhenius-Gleichgewichtsbeziehung)
K = K_0 * exp ( - DeltaG_HB / (R * T) )
- K ist die Gleichgewichtskonstante der Wasserstoffbrückenbildung
- K_0 ist ein präexponentieller Faktor
- DeltaG_HB ist die freie Gibbs-Energie der Wasserstoffbrückenbindung (J/mol)
- R ist die universelle Gaskonstante (J/(mol·K))
- T ist die Temperatur in (K)
Wasserstoffbrücken sind schwächer als kovalente Bindungen, aber deutlich stärker als reine van-der-Waals-Kräfte. Sie führen zu einer gerichteten Anziehung zwischen Molekülen und beeinflussen deren räumliche Anordnung. Dadurch prägen sie viele physikalische Eigenschaften von Stoffen.
In der Verfahrenstechnik spielen Wasserstoffbrücken eine wichtige Rolle bei Flüssigkeiten, Lösungen und Polymeren. Sie beeinflussen die Viskosität, die Gelbildung, die Löslichkeit und das Quellverhalten. Besonders Wasser, Alkohole, Stärke, Cellulosederivate und viele Verdickungsmittel zeigen ausgeprägte Wasserstoffbrückenbindungen.
Wasserstoffbrücken sind temperaturabhängig. Mit steigender Temperatur werden sie teilweise aufgelöst. Dies erklärt Viskositätsabnahmen, Strukturänderungen und Phasenübergänge bei Erwärmung. Auch mechanische Scherung kann Wasserstoffbrücken vorübergehend lösen.
Beim Mischen, Temperieren und Trocknen beeinflussen Wasserstoffbrücken das Prozessverhalten daher maßgeblich. Sie bestimmen, wie Stoffe miteinander wechselwirken und wie stabil gebildete Stoffstrukturen sind.

