Enlaces de hidrógeno
Los enlaces de hidrógeno son interacciones intermoleculares específicas entre un átomo de hidrógeno y un átomo muy electronegativo, como el oxígeno, el nitrógeno o el flúor. En este caso, el átomo de hidrógeno está unido covalentemente a un átomo electronegativo e interactúa además con un par de electrones libres de una molécula vecina.
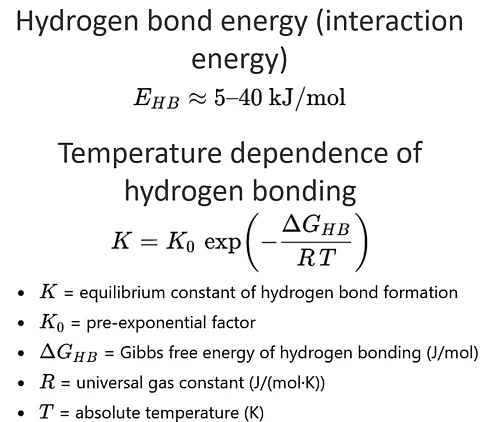
Energía de enlace de hidrógeno (rango típico)
E_HB ≈ 5 – 40 kJ/mol
- E_HB es la energía de enlace de hidrógeno
- Los valores típicos dependen del par donante-aceptor
Dependencia de la temperatura del enlace de hidrógeno (relación de equilibrio de Arrhenius)
K = K_0 * exp ( - DeltaG_HB / (R * T) )
- K es la constante de equilibrio de la formación de puentes de hidrógeno
- K_0 es un factor preexponencial
- DeltaG_HB es la energía libre de Gibbs del enlace de hidrógeno (J/mol)
- R es la constante universal de los gases (J/(mol·K))
- T es la temperatura en (K)
Los enlaces de hidrógeno son más débiles que los enlaces covalentes, pero considerablemente más fuertes que las simples fuerzas de van der Waals. Dan lugar a una atracción direccional entre las moléculas e influyen en su disposición espacial. De este modo, determinan muchas de las propiedades físicas de las sustancias.
En la ingeniería de procesos, los enlaces de hidrógeno desempeñan un papel importante en los líquidos, las soluciones y los polímeros. Influyen en la viscosidad, la gelificación, la solubilidad y el comportamiento de hinchamiento. En particular, el agua, los alcoholes, el almidón, los derivados de la celulosa y muchos espesantes presentan enlaces de hidrógeno muy marcados.
Los enlaces de hidrógeno dependen de la temperatura. A medida que aumenta la temperatura, se rompen parcialmente. Esto explica la disminución de la viscosidad, los cambios estructurales y las transiciones de fase que se producen al calentar. El cizallamiento mecánico también puede romper temporalmente los enlaces de hidrógeno.
Por lo tanto, durante las fases de mezcla, templado y secado, los enlaces de hidrógeno influyen de manera decisiva en el comportamiento del proceso. Determinan cómo interactúan las sustancias entre sí y el grado de estabilidad de las estructuras que se forman.

