수소 결합
수소 결합은 수소 원자와 강한 전기음성 원자(예: 산소, 질소 또는 플루오린) 사이의 특수한 분자 간 상호작용이다. 이때 수소 원자는 전기음성 원자에 공유 결합되어 있으며, 인접한 분자의 자유 전자쌍과 추가로 상호 작용한다.
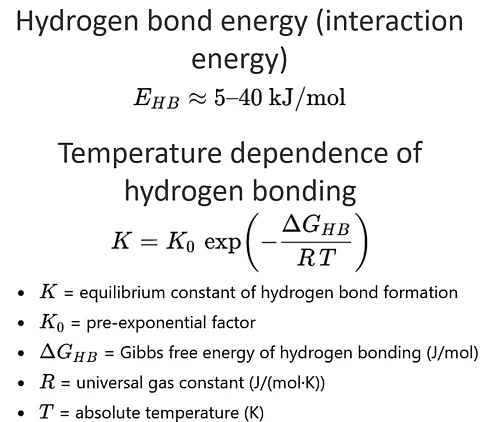
수소 결합 에너지(전형적인 범위)
E_HB ≈ 5 – 40 kJ/mol
- E_HB는 수소 결합 에너지이다
- 전형적인 값은 도너–액셉터 쌍에 따라 달라진다
수소 결합의 온도 의존성(아레니우스 평형 관계식)
K = K_0 * exp ( - DeltaG_HB / (R * T) )
- K는 수소 결합 형성의 평형 상수이다
- K_0는 전지수 인자이다
- DeltaG_HB는 수소 결합의 깁스 자유 에너지(J/mol)이다
- R은 보편 기체 상수(J/(mol·K))이다
- T는 온도(K)이다
수소 결합은 공유 결합보다 약하지만, 순수한 반데르발스 힘보다 훨씬 강하다. 이는 분자 사이에 방향성을 가진 인력을 유도하고, 그들의 공간적 배열에 영향을 미친다. 이로 인해 물질의 많은 물리적 특성이 결정된다.
공정공학에서 수소 결합은 액체, 용액 및 고분자에서 중요한 역할을 한다. 이는 점도, 겔 형성, 용해도 및 팽윤 거동에 영향을 미친다. 특히 물, 알코올, 전분, 셀룰로스 유도체 및 많은 증점제는 뚜렷한 수소 결합을 보인다.
수소 결합은 온도에 의존한다. 온도가 상승하면 일부가 부분적으로 끊어진다. 이는 가열 시 점도 감소, 구조 변화 및 상전이를 설명한다. 기계적 전단 역시 수소 결합을 일시적으로 끊을 수 있다.
따라서 혼합, 온도 조절 및 건조에서 수소 결합은 공정 거동에 결정적으로 영향을 미친다. 이는 물질들이 서로 어떻게 상호작용하는지와 형성된 물질 구조가 얼마나 안정한지를 좌우한다.

