Wiązania wodorowe
Wiązania wodorowe to szczególne oddziaływania międzycząsteczkowe zachodzące między atomem wodoru a atomem o wysokiej elektroujemności, na przykład tlenem, azotem lub fluorem. W tym przypadku atom wodoru jest związany kowalencyjnie z atomem elektroujemnym i dodatkowo oddziałuje z wolną parą elektronów sąsiedniej cząsteczki.
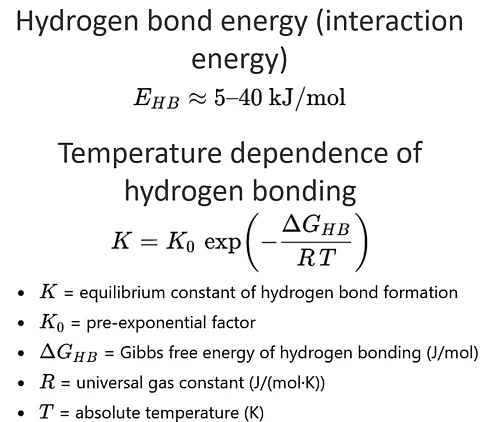
Energia wiązania wodorowego (typowy zakres)
E_HB ≈ 5 – 40 kJ/mol
- E_HB to energia wiązania wodorowego
- Typowe wartości zależą od pary donor-akceptor
Zależność wiązania wodorowego od temperatury (równanie równowagi Arrheniusa)
K = K_0 * exp ( - DeltaG_HB / (R * T) )
- K to stała równowagi tworzenia wiązań wodorowych
- K_0 jest współczynnikiem przedpotęgiowym
- DeltaG_HB to energia swobodna wiązania wodorowego (J/mol)
- R to uniwersalna stała gazowa (J/(mol·K))
- T to temperatura w kelwinach (K)
Wiązania wodorowe są słabsze od wiązań kowalencyjnych, ale znacznie silniejsze od samych sił van der Waalsa. Powodują one ukierunkowane przyciąganie między cząsteczkami i wpływają na ich rozmieszczenie w przestrzeni. W ten sposób determinują wiele właściwości fizycznych substancji.
W inżynierii procesowej wiązania wodorowe odgrywają istotną rolę w przypadku cieczy, roztworów i polimerów. Wpływają one na lepkość, żelowanie, rozpuszczalność oraz właściwości pęcznienia. Szczególnie woda, alkohole, skrobia, pochodne celulozy i wiele środków zagęszczających wykazują wyraźne wiązania wodorowe.
Wiązania wodorowe są zależne od temperatury. Wraz ze wzrostem temperatury ulegają one częściowemu rozpadowi. Wyjaśnia to spadek lepkości, zmiany struktury oraz przemiany fazowe zachodzące podczas ogrzewania. Również ścinanie mechaniczne może tymczasowo rozrywać wiązania wodorowe.
Podczas mieszania, temperowania i suszenia wiązania wodorowe mają zatem decydujący wpływ na przebieg procesu. Określają one, w jaki sposób substancje oddziałują na siebie oraz jak stabilne są powstałe struktury.

