水素結合
水素結合とは、水素原子と、酸素、窒素、フッ素などの電気陰性度の高い原子との間に生じる特殊な分子間相互作用である。この際、水素原子は電気陰性度の高い原子と共有結合で結びついているほか、隣接する分子の遊離電子対とも相互作用する。
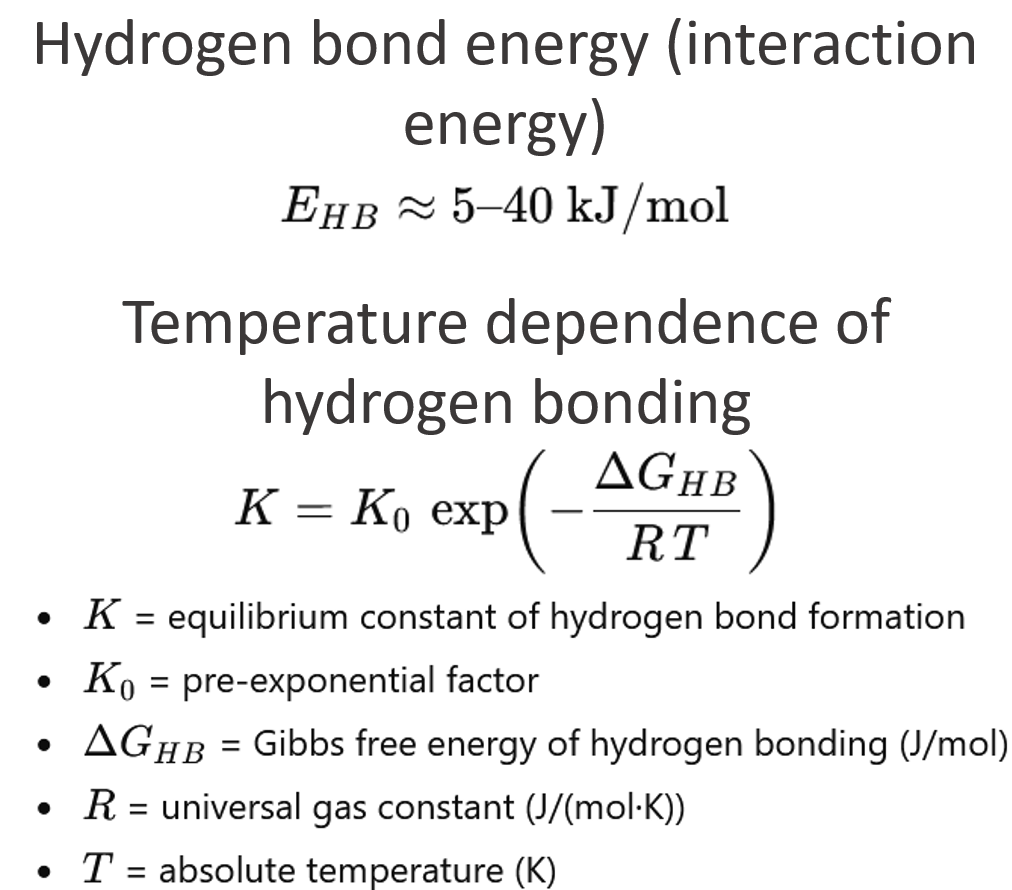
水素結合エネルギー(典型的な範囲)
E_HB ≈ 5 – 40 kJ/mol
- E_HBは水素結合エネルギーである
- 典型的な値はドナー・アクセプター対によって異なる
水素結合の温度依存性(アレニウス平衡式)
K = K_0 * exp ( - DeltaG_HB / (R * T) )
- Kは水素結合の平衡定数である
- K_0 は指数関数的な因子である
- DeltaG_HB は、水素結合の自由ギブズエネルギー(J/mol)である
- R は普遍的な気体定数(J/(mol·K))である
- Tは温度(K)である
水素結合は共有結合よりも弱いものの、純粋なファンデルワールス力よりははるかに強い。水素結合は分子間に方向性のある引力を生じさせ、分子の空間的な配列に影響を与える。そのため、物質の多くの物理的性質を決定づけている。
プロセス工学において、水素結合は液体、溶液、および高分子において重要な役割を果たしています。これらは粘度、ゲル化、溶解度、および膨潤挙動に影響を与えます。特に水、アルコール、デンプン、セルロース誘導体、および多くの増粘剤は、顕著な水素結合を示します。
水素結合は温度に依存する。温度が上昇すると、水素結合は部分的に解ける。これが、加熱に伴う粘度の低下、構造の変化、および相転移を説明している。また、機械的なせん断力によっても、水素結合が一時的に解けることがある。
したがって、混合、テンパリング、乾燥の各工程において、水素結合はプロセスの挙動に決定的な影響を及ぼします。水素結合は、物質同士がどのように相互作用するか、また形成された物質構造がどれほど安定しているかを決定づけるのです。

