Водородные связи
Водородные связи — это особые межмолекулярные взаимодействия между атомом водорода и атомом с высокой электроотрицательностью, например кислорода, азота или фтора. При этом атом водорода ковалентно связан с электроотрицательным атомом и дополнительно взаимодействует со свободной парой электронов соседней молекулы.
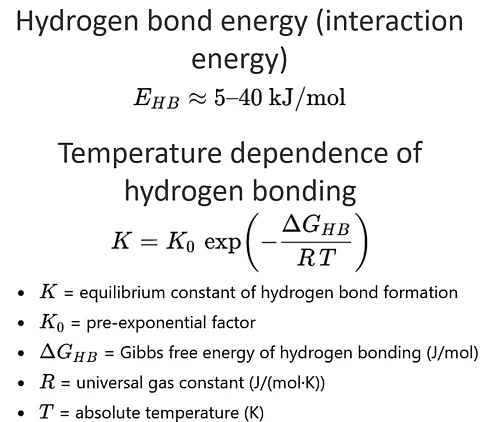
Энергия водородных связей (типичный диапазон)
E_HB ≈ 5 – 40 kJ/mol
- E_HB — энергия водородной связи
- Типичные значения зависят от пары «донор-акцептор»
Зависимость водородной связи от температуры (уравнение равновесия Аррениуса)
K = K_0 * exp ( - DeltaG_HB / (R * T) )
- K — константа равновесия образования водородных связей
- K_0 — это преэкспоненциальный коэффициент
- DeltaG_HB — свободная энергия Гиббса водородной связи (Дж/моль)
- R — универсальная газовая постоянная (Дж/(моль·К))
- T — температура в (К)
Водородные связи слабее ковалентных связей, но значительно сильнее, чем простые ван-дер-ваальсовые силы. Они приводят к направленному притяжению между молекулами и влияют на их пространственное расположение. Таким образом, они определяют многие физические свойства веществ.
В технологическом производстве водородные связи играют важную роль в поведении жидкостей, растворов и полимеров. Они влияют на вязкость, гелеобразование, растворимость и способность к набуханию. Особенно выраженные водородные связи наблюдаются в воде, спиртах, крахмале, производных целлюлозы и многих загустителях.
Водородные связи зависят от температуры. При повышении температуры они частично разрушаются. Это объясняет снижение вязкости, изменения структуры и фазовые переходы при нагревании. Механическое сдвиговое усилие также может временно разрушать водородные связи.
Поэтому при смешивании, термообработке и сушке водородные связи оказывают существенное влияние на ход процесса. Они определяют, как вещества взаимодействуют друг с другом и насколько стабильны образующиеся структуры веществ.

