legami a idrogeno
I legami idrogeno sono particolari interazioni intermolecolari tra un atomo di idrogeno e un atomo fortemente elettronegativo, come l'ossigeno, l'azoto o il fluoro. In questo caso, l'atomo di idrogeno è legato in modo covalente a un atomo elettronegativo e interagisce inoltre con una coppia di elettroni liberi di una molecola vicina.
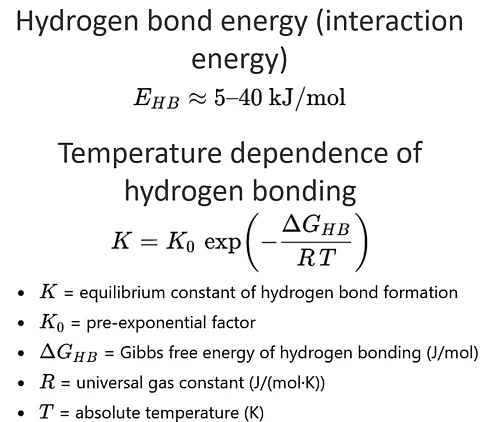
Energia dei legami idrogeno (intervallo tipico)
E_HB ≈ 5 – 40 kJ/mol
- E_HB è l'energia di legame idrogeno
- I valori tipici dipendono dalla coppia donatore-accettore
Dipendenza dalla temperatura del legame idrogeno (relazione di equilibrio di Arrhenius)
K = K_0 * exp ( - DeltaG_HB / (R * T) )
- K è la costante di equilibrio della formazione dei ponti idrogeno
- K_0 è un fattore preesponenziale
- DeltaG_HB è l'energia libera di Gibbs del legame a ponte idrogeno (J/mol)
- R è la costante universale dei gas (J/(mol·K))
- T è la temperatura in (K)
I legami a ponte idrogeno sono più deboli dei legami covalenti, ma nettamente più forti delle semplici forze di van der Waals. Essi determinano un’attrazione direzionata tra le molecole e ne influenzano la disposizione spaziale. In questo modo determinano molte proprietà fisiche delle sostanze.
Nell'ingegneria dei processi, i legami idrogeno svolgono un ruolo importante nei liquidi, nelle soluzioni e nei polimeri. Influenzano la viscosità, la gelificazione, la solubilità e il comportamento di rigonfiamento. In particolare, l'acqua, gli alcoli, l'amido, i derivati della cellulosa e molti addensanti presentano legami idrogeno marcati.
I legami idrogeno dipendono dalla temperatura. Con l'aumentare della temperatura, essi si rompono parzialmente. Ciò spiega la diminuzione della viscosità, i cambiamenti strutturali e le transizioni di fase in seguito al riscaldamento. Anche lo sforzo di taglio meccanico può rompere temporaneamente i legami idrogeno.
Durante le fasi di miscelazione, tempra e essiccazione, i legami idrogeno influenzano quindi in modo determinante l'andamento del processo. Essi determinano il modo in cui le sostanze interagiscono tra loro e il grado di stabilità delle strutture che si formano.

