Verdampfungsenthalpie
Die Verdampfungsenthalpie beschreibt die spezifische Energie, die erforderlich ist, um eine Flüssigkeit bei konstanter Temperatur und konstantem Druck zu verdampfen. Sie beschreibt den Phasenübergang von der flüssigen in die gasförmige Phase. Die Verdampfungsenthalpie ist stoff- und temperaturabhängig.
In der Verfahrenstechnik ist die Verdampfungsenthalpie eine Schlüsselgröße für Trocknungsprozesse, Verdampfer, Destillation und Vakuumtrocknung. Sie bestimmt den Energiebedarf eines Prozesses und beeinflusst die Auslegung von Heizflächen und Energieversorgung.
Der Wärmebedarf für die Verdampfung wird durch folgende Gleichung beschrieben:
Q_dot =m_dot * Delta_h_vap
- Q_dot = Wärmefluss oder Wärmebedarf (W)
- m_dot = Massenstrom der verdampften Flüssigkeit (kg/s)
- Delta_h_vap = Verdampfungsenthalpie (J/kg))
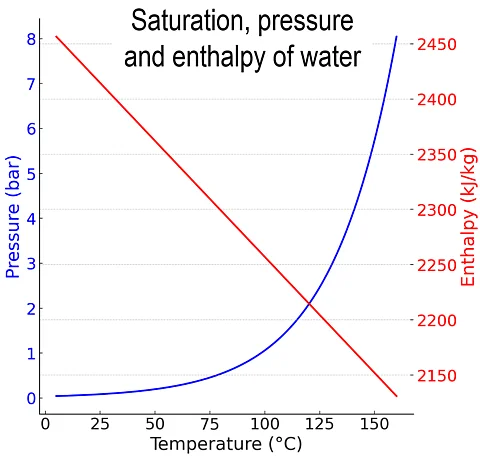
Die Verdampfungsenthalpie beträgt bei Wasser bei 100 °C etwa 2257 kJ/kg und nimmt mit steigender Temperatur ab. Unter Vakuum bleibt die Verdampfungsenthalpie nahezu konstant, während der Siedepunkt sinkt.
In Trocknern und Vakuum-Kontakttrocknern ist die Verdampfungsenthalpie häufig der dominierende Energieanteil. Sie bestimmt die minimale theoretische Energie, die zur Entfeuchtung eines Produkts benötigt wird.

