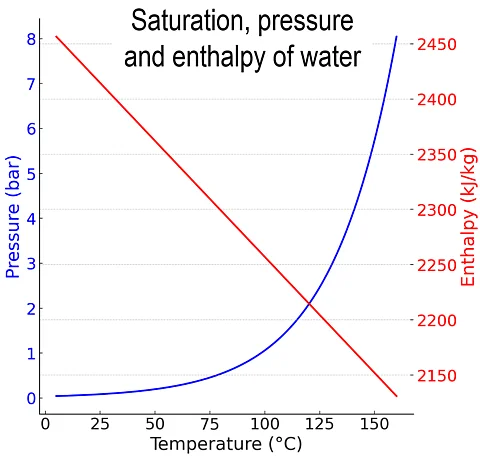
entalpía de vaporización
La entalpía de vaporización describe la energía específica necesaria para evaporar un líquido a temperatura y presión constantes. Describe la transición de fase de la fase líquida a la fase gaseosa. La entalpía de vaporización depende de la sustancia y de la temperatura.
En la ingeniería de procesos, la entalpía de vaporización es una magnitud clave para los procesos de secado, los evaporadores, la destilación y el secado al vacío. Determina la demanda de energía de un proceso e influye en el dimensionamiento de las superficies de calentamiento y el suministro de energía.
El requerimiento de calor para la evaporación se describe mediante la siguiente ecuación:
Q_dot =m_dot * Delta_h_vap
- Q_dot = flujo de calor o demanda de calor (W)
- m_dot = caudal másico del líquido evaporado (kg/s)
- Delta_h_vap = entalpía de vaporización (J/kg))
La entalpía de vaporización del agua a 100 °C es de aproximadamente 2257 kJ/kg y disminuye con el aumento de la temperatura. Bajo vacío, la entalpía de vaporización permanece casi constante, mientras que el punto de ebullición disminuye.
En secadores y secadores de contacto al vacío, la entalpía de vaporización suele ser la fracción de energía dominante. Determina la energía teórica mínima necesaria para deshumidificar un producto.

