enthalpie de vaporisation
L’enthalpie de vaporisation décrit l’énergie spécifique nécessaire pour vaporiser un liquide à température et pression constantes. Elle décrit le changement de phase de l’état liquide à l’état gazeux. L’enthalpie de vaporisation dépend de la substance et de la température.
En génie des procédés, l’enthalpie de vaporisation est une grandeur clé pour les procédés de séchage, les évaporateurs, la distillation et le séchage sous vide. Elle détermine la demande énergétique d’un procédé et influence la conception des surfaces de chauffage et l’approvisionnement en énergie.
Le besoin de chaleur pour la vaporisation est décrit par l’équation suivante:
Q_dot =m_dot * Delta_h_vap
- Q_dot = flux de chaleur ou besoin de chaleur (W)
- m_dot = débit massique du liquide vaporisé (kg/s)
- Delta_h_vap = enthalpie de vaporisation (J/kg))
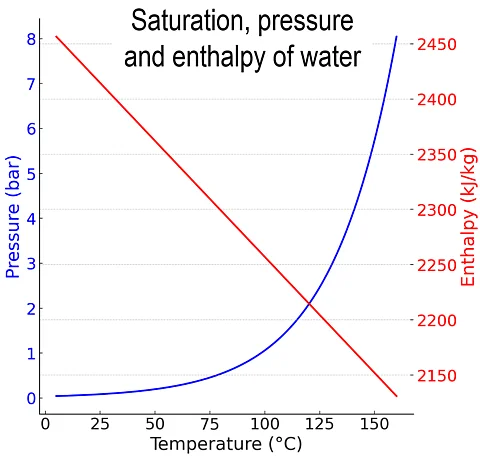
Pour l’eau à 100°C, l’enthalpie de vaporisation est d’environ 2257 kJ/kg et diminue avec l’augmentation de la température. Sous vide, l’enthalpie de vaporisation reste presque constante, tandis que le point d’ébullition diminue.
Dans les séchoirs et les séchoirs sous vide à contact, l’enthalpie de vaporisation est souvent la part d’énergie dominante. Elle détermine l’énergie théorique minimale nécessaire pour déshumidifier un produit.

