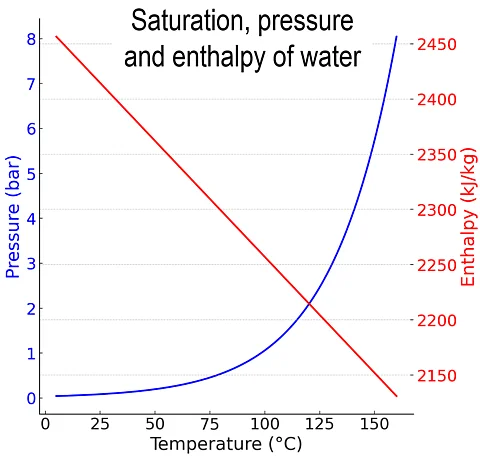
entalpia di vaporizzazione
L'entalpia di vaporizzazione descrive l'energia specifica necessaria per vaporizzare un liquido a temperatura e pressione costanti. Descrive il passaggio di fase dallo stato liquido a quello gassoso. L'entalpia di vaporizzazione dipende dalla sostanza e dalla temperatura.
Nell'ingegneria di processo l'entalpia di vaporizzazione è un parametro chiave per i processi di essiccazione, gli evaporatori, la distillazione e l'essiccazione sotto vuoto. Determina il fabbisogno energetico di un processo e influisce sul dimensionamento delle superfici di riscaldamento e dell'approvvigionamento energetico.
Il fabbisogno di calore per la vaporizzazione è descritto dalla seguente equazione:
Q_dot =m_dot * Delta_h_vap
- Q_dot = flusso di calore o fabbisogno di calore (W)
- m_dot = portata massica del liquido vaporizzato (kg/s)
- Delta_h_vap = entalpia di vaporizzazione (J/kg))
Per l'acqua a 100 °C l'entalpia di vaporizzazione è di circa 2257 kJ/kg e diminuisce con l'aumentare della temperatura. Sotto vuoto l'entalpia di vaporizzazione rimane pressoché costante, mentre il punto di ebollizione diminuisce.
Negli essiccatori e negli essiccatori a contatto sotto vuoto l'entalpia di vaporizzazione è spesso la componente energetica dominante. Determina l'energia teorica minima necessaria per la deumidificazione di un prodotto.

