Método del isoteniscopio
El método del isoteniscopio es un método de medición físico-químico para determinar la presión de vapor de un líquido en función de la temperatura. Es uno de los métodos estáticos de determinación de la presión de vapor y se utiliza en particular en termodinámica y en el diseño de ingeniería de procesos de evaporación.
En la tecnología de procesamiento, la evaporación de líquidos es un paso clave del proceso, por ejemplo para la concentración, la cristalización o la separación de sustancias sensibles a la temperatura. Otro ejemplo es la producción alimentaria o farmacéutica, donde los componentes sensibles al calor deben separarse suavemente. Otro campo de aplicación es la recuperación de disolventes de los residuos durante la rectificación.
La eficacia y la carga térmica del producto dependen fundamentalmente del comportamiento de ebullición del líquido. Éste, a su vez, se ve influido por la presión de vapor, que cambia con la temperatura.
La presión de vapor define la presión a la que el líquido está en equilibrio con su propia fase de vapor. Al aumentar la temperatura, aumenta la presión de vapor y se desplaza el punto de ebullición bajo una presión ambiente dada. Por tanto, en los sistemas técnicos, especialmente en condiciones de vacío o en sistemas de evaporación multietapa, es esencial conocer con precisión la curva de presión de vapor.
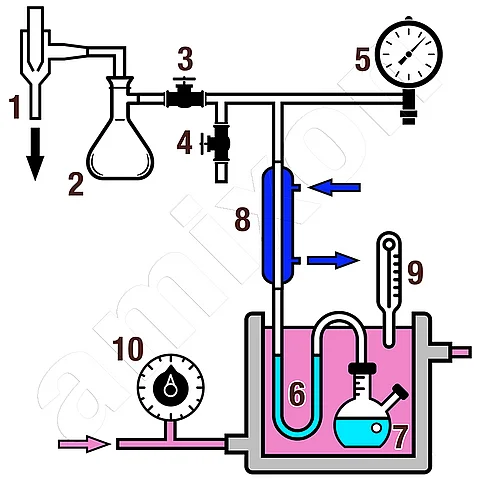
Un isoteniscopio es un dispositivo de medición sencillo pero preciso fabricado en vidrio. Consiste en un sistema de tubos en forma de U que se llenan parcialmente con el líquido que se va a analizar y un líquido de referencia (a menudo mercurio). La muestra se calienta en un baño con termostato, mientras que la presión del sistema se controla mediante vacío o una atmósfera de gas conocida. La presión de equilibrio del líquido puede determinarse entonces por la diferencia de altura de las columnas de mercurio. El valor medido corresponde a la presión de vapor de equilibrio de la muestra a la temperatura respectiva. Las mediciones repetidas a diferentes temperaturas dan lugar a una curva de presión de vapor. A partir de esta curva, pueden determinarse variables termodinámicas como la entalpía de vaporización mediante linealización según la ecuación de Clausius-Clapeyron.
ln(p) = −ΔHvap /(R · T) + C
p : Presión de vapor
ΔHvap : Entalpía de vaporización
R : Constante universal de los gases
T : temperatura absoluta
C : Constante de integración
En el centro técnico de amixon encontrará secadores de mezcla al vacío y plantas de evaporación. Pueden utilizarse para pruebas de procesos y desarrollo de productos.

